
|

|

|

|

|
|||
| Descripción |
|
Esta asignatura se imparte en el 1er cuatrimestre del 1er curso de Ingeniería Industrial. Consta de 7,5 créditos (4 créditos de teoría y 3,5 de prácticas). Es una asignatura de carácter básico cuyo fin es establecer las bases científicas necesarias para la formación del Ingeniero Industrial en la Industria Química y en la Tecnología del Medio Ambiente. Sus contenidos son imprescindibles para el estudio y comprensión de un buen número de
asignaturas correspondientes a la titulación de Ingeniería Industrial
tanto de carácter troncal u obligatorio como optativas o de libre
elección. |
|
|
|
Que comprenda los principios de la Termodinámica para poder aplicarlos a los procesos químicos. Que conozca la cinética de las reacciones químicas y su implicación en la economía de los procesos químicos industriales. Que sea capaz de relacionar los fundamentos científicos de las reacciones ácido-base con su aplicación a procesos de interés industrial. Que conozca las aplicaciones industriales de los equilibrios de solubilidad-precipitación. Que comprenda los fundamentos científicos de los procesos de oxidación-reducción y que sepa aplicarlos a los procesos industriales. Que conozca la importancia de la Química en la Industria. |
| Conocimientos previos |
|
Para un seguimiento óptimo del programa es necesario que el alumno conozca y sepa manejar una serie de aspectos básicos tales como:
En la dirección: http://www.eis.uva.es/qgintro tenemos un Aula Virtual en la que se encuentra una descripción de todos estos temas tanto desde un punto de vista teórico (tutoriales) como práctico (ejercicios). En esta Aula Virtual se puede hacer también un test de cada uno de los temas. |
| Programa de la asignatura |
|
Programa de Teoría: |
|
|
|
|
|
|
|
|
||||||||||||||||||||||||||||||||
|
Las prácticas consisten en 7 sesiones.
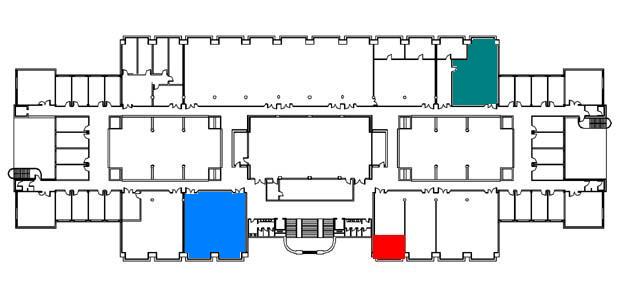
5 sesiones de 4 horas (16-20 h)
en el Laboratorio de Química General (2ª planta, zona azul en el dibujo), en las que se realizarán las siguientes prácticas: |
||||||||||||||||||||||||||||||||
 |
||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||
|
Enlaces relacionados: Conferencia sobre "Prevención de Riesgos" impartida por Dª María Dolores Miñambres del Moral, Ingeniero Industrial y Directora del Servicio de Prevención de Riesgos Laborales de la Universidad de Valladolid Seguridad y Prevención en el Laboratorio Químico,
por Francisco J. García Alonso de la Universidad de Oviedo. |
||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||
|
|
| Organización de la asignatura |
|
Horario |
| Grupo 2: Lunes, martes,
jueves y viernes de 11-12 h. Aula B-2
|
|
Aula Virtual |
|
El desarrollo del curso lo seguiremos mediante la plataforma educativa MOODLE que pone a nuestra disposición la E.T.S.I.I. el enlace es e-duca.eis.uva.es. El acceso está restringido a los alumnos de este grupo. Una vez dentro de la plataforma elegiremos el curso: "Fundamentos Químicos de la Ingeniería (Grupo 2). Para entrar hay que identificarse mediante un "nombre de usuario" que corresponde al DNI (8 dígitos y una letra), y una "contraseña" que corresponde al NIA. Dentro de este espacio virtual pondremos toda la información relevante del curso, los cuestionarios, trabajos, etc.. |
|
Exámenes |
| Examen ordinario: 25 de Enero de 2010
Examen extraordinario: La hora y la distribución de los alumnos en las aulas se publicará en el tablón de anuncios del departamento de Química Orgánica (2ª planta) unos días antes del examen.
|
| Materiales de apoyo |
|
|
Visita la página web del libro (optimizado para Microsoft Internet Explorer) |
|
|
|
Principios de Química (Los caminos del descubrimiento); 3ª edición. Química; 9ª edición. Química (la ciencia central); 9ª edición. INICIACIÓN A LA QUÍMICA SUPERIOR: Fundamentos de enlace y estructura de la materia. Ed.: ANAYA Problemas: Fundamentos y problemas de Química. 1000 problemas de Química General. Química General. Formulación: Formulación y Nomenclatura. Química Inorgánica. |
|
|
|
Un Laboratorio Virtual que es una simulación de un Laboratorio de química, desarrollado en la Universidad Carnegie Mellon (USA), que permite a los estudiantes combinar diferentes disoluciones y observar los resultados de sus experimentos. Una Bomba Calorimétrica de Oxígeno, este applet simula la combustión de una sustancia y la medida del calor desprendido en esta reacción dentro de un calorímetro. Ha sido creado por Gary L. Bertrand de la Universidad Missouri-Rolla (USA) y traducido por Santiago Aparicio de la Universidad de Burgos. |
| Tutorías |
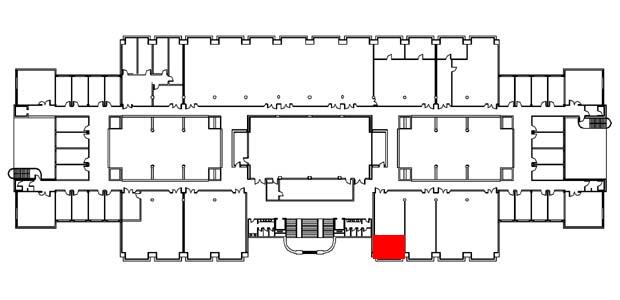
| Lunes, martes y jueves de
10-11 h. y de 12-13 h. Laboratorio de Modelización Molecular (2º planta, zona roja en el dibujo) También se pueden concertar citas fuera del horario oficial bien por teléfono
|
 |
| Convocatorias y novedades |